03-Devoir de géométrie N°3
5 participants
Page 1 sur 1
 03-Devoir de géométrie N°3
03-Devoir de géométrie N°3
Bonsoir !
Finalement, contrairement à ce que je vous ai annoncé lors du devoir N°2, nous allons d'abord étudier autre chose aujourd'hui.
Vous vous souvenez de notre premier devoir de géométrie ou nous avions parlé du cube, de 2 tétraèdres inscrits et de l’octaèdre qui apparaissait à l’intersection des 2 tétraèdres. Aujourd’hui, je vais vous raconter comment les épis de maïs ont découvert le dodécaèdre régulier.
C’était un beau jour de printemps ou nous devisions entre épis devant une belle sphère de la taille d’une bille. Ce jour-là, plusieurs abeilles vinrent et entreprirent de construire des alvéoles sur la sphère. C’était la première fois qu’elles se lançaient dans une telle aventure, aussi les entendîmes-nous fredonner longtemps avant de se mettre à l’ouvrage. Elles finirent par décider d’attaquer leur chantier en s’imposant de toujours construire trois parois unies en un point à 120°. Pas folle, les guêpes, elles avaient calculé la taille de chaque paroi afin que toute la bille fût correctement couverte.
Quelle ne fut pas leur surprise, et la nôtre !
Les alvéoles n’étaient pas hexagonales mais pentagonales !
Incroyable !
Sur un plan, la somme des angles
- d’un hexagone : 4π
- d’un pentagone : 3π
- d’un quadrilatère : 2π
- d’un triangle : π
Sur la sphère, en prenant des angles égaux à 120°, on peut construire 12 alvéoles pentagonales !
Dans ce cas, la somme des angles de ces pentagones est égale à 600°, soit encore 10/3 π.
Elle est donc elle aussi supérieure à celle obtenue sur un plan (3π).
Je vous demande de travailler un peu plus aujourd’hui. Vous allez :
1- dessiner un dodécaèdre régulier et le déposer dans votre réponse ;
2- dessiner son dual, l’icosaèdre, dont les sommets se trouvent au centre des 12 faces du dodécaèdre régulier, et le déposer dans votre réponse.
3- Vous devrez établir une égalité (qui fonctionne pour les 2 solides) qui relie le nombre S de sommets, A d’arêtes et F de faces.
4- Vous devez indiquer le nombre de dodécaèdres différents à symétrie centrale qui existent.
Allez ! Au travail...
Finalement, contrairement à ce que je vous ai annoncé lors du devoir N°2, nous allons d'abord étudier autre chose aujourd'hui.
Vous vous souvenez de notre premier devoir de géométrie ou nous avions parlé du cube, de 2 tétraèdres inscrits et de l’octaèdre qui apparaissait à l’intersection des 2 tétraèdres. Aujourd’hui, je vais vous raconter comment les épis de maïs ont découvert le dodécaèdre régulier.
C’était un beau jour de printemps ou nous devisions entre épis devant une belle sphère de la taille d’une bille. Ce jour-là, plusieurs abeilles vinrent et entreprirent de construire des alvéoles sur la sphère. C’était la première fois qu’elles se lançaient dans une telle aventure, aussi les entendîmes-nous fredonner longtemps avant de se mettre à l’ouvrage. Elles finirent par décider d’attaquer leur chantier en s’imposant de toujours construire trois parois unies en un point à 120°. Pas folle, les guêpes, elles avaient calculé la taille de chaque paroi afin que toute la bille fût correctement couverte.
Quelle ne fut pas leur surprise, et la nôtre !
Les alvéoles n’étaient pas hexagonales mais pentagonales !
Incroyable !
Sur un plan, la somme des angles
- d’un hexagone : 4π
- d’un pentagone : 3π
- d’un quadrilatère : 2π
- d’un triangle : π
Sur la sphère, en prenant des angles égaux à 120°, on peut construire 12 alvéoles pentagonales !
Dans ce cas, la somme des angles de ces pentagones est égale à 600°, soit encore 10/3 π.
Elle est donc elle aussi supérieure à celle obtenue sur un plan (3π).
Je vous demande de travailler un peu plus aujourd’hui. Vous allez :
1- dessiner un dodécaèdre régulier et le déposer dans votre réponse ;
2- dessiner son dual, l’icosaèdre, dont les sommets se trouvent au centre des 12 faces du dodécaèdre régulier, et le déposer dans votre réponse.
3- Vous devrez établir une égalité (qui fonctionne pour les 2 solides) qui relie le nombre S de sommets, A d’arêtes et F de faces.
4- Vous devez indiquer le nombre de dodécaèdres différents à symétrie centrale qui existent.
Allez ! Au travail...
Dernière édition par SansOgm le Dim 18 Déc - 23:47, édité 1 fois

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Mes abeilles m'ont construit des alvéoles à 2 côtés. Elles m'ont expliqué que c'était parfaitement cohérent avec les 120° de départ et le souhait de se rapprocher de l'hexagone.

Alexandre- Messages : 224
Date d'inscription : 24/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Cher Alexandre, vos abeilles ont du miel aux pattes !
Vous n'êtes pas tombé sur des ouvrières; vos abeilles sont du genre à clore le sujet, je vois.
Trouvez de bonnes ouvrières, elles ne molliront pas la cire ainsi !
Vous n'êtes pas tombé sur des ouvrières; vos abeilles sont du genre à clore le sujet, je vois.
Trouvez de bonnes ouvrières, elles ne molliront pas la cire ainsi !

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Non, je délègue !Je vous demande de travailler
Mes abeilles ne sont pas des feignasses, elles ont fait un compromis entre leur habituel rayon de miel plan au tapis hexagonal comme une couche de graphite et le dodécaèdre tapissé de 12 cellules pentagonales.
Elles ont réalisé un nano-ballon de foot avec 32 cellules, 12 pentagonales et 20 hexagonales, synthétisant ainsi un beau fullerène C₆₀. Ce sont des artistes !

Note que les tiennes n'ont pas totalement démérité puisqu'elles ont fait un fullerène C₂₀.
.

Tchernobilly the kid- Messages : 947
Date d'inscription : 11/07/2016
Age : 76
Localisation : midi moins le quart
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
J'ai pas envie de travailler... Et puis, c'est pas marrant les dodécaèdres.
SansOgm, vous voulez pas qu'on regarde une vidéo sur la géométrie et la mode ?
Oui, vous êtes d'accord : Chouette !
Alors, regardons
http://savoirs.ens.fr/expose.php?id=1731
SansOgm, vous voulez pas qu'on regarde une vidéo sur la géométrie et la mode ?
Oui, vous êtes d'accord : Chouette !
Alors, regardons
http://savoirs.ens.fr/expose.php?id=1731

saint-marc- Messages : 852
Date d'inscription : 05/09/2016
Age : 66
Localisation : Poitiers
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
La vidéo sur la géométrie et la mode était très intéressante !
Elles vous a permis de voir que la géométrie est beaucoup plus riche qu'on ne l'imagine : Magnifiques sont ces robes développables du styliste de mode japonais Issey Miyaké !

Mais, revenons à nos polyèdres, dont ceux de ce devoir : Le dodécaèdre régulier à 12 faces pentagonales et son dual, l'icosaèdre à 20 faces triangulaires, que vous avez vu dans la même vidéo

Allez-vous répondre aux questions 3 et 4 ?
Elles vous a permis de voir que la géométrie est beaucoup plus riche qu'on ne l'imagine : Magnifiques sont ces robes développables du styliste de mode japonais Issey Miyaké !

Mais, revenons à nos polyèdres, dont ceux de ce devoir : Le dodécaèdre régulier à 12 faces pentagonales et son dual, l'icosaèdre à 20 faces triangulaires, que vous avez vu dans la même vidéo

Allez-vous répondre aux questions 3 et 4 ?
Dernière édition par SansOgm le Mar 22 Nov - 11:25, édité 1 fois (Raison : Agrandissement des photos des robes)

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
3 ...
Le dodécaèdre a :
12 faces (c'est pas un scoop)
20 sommets (comme le fullerène C₂₀) mais ce ne sont pas nécessairement des atomes de carbone.
Nombre d'arêtes : un pentagone a 5 côtés (c'est pas un scoop), il y a 12 pentagones et chaque arête est commune à deux pentagones -> 5x12/2 = 30 arêtes.
Donc F=12, S=20, A=30
L'icosaèdre dual du dodécaèdre -> on remplace les sommets par des faces et réciproquement
S = 12
F = 20
A inchangé. On vérifie :
20 faces avec 3 côtés communs
A = 20x3/2 = 30
Dans les deux cas, la somme S+F+A est la même (62).
4 ...
Ça m'suffit pour le moment
.
Le dodécaèdre a :
12 faces (c'est pas un scoop)
20 sommets (comme le fullerène C₂₀) mais ce ne sont pas nécessairement des atomes de carbone.
Nombre d'arêtes : un pentagone a 5 côtés (c'est pas un scoop), il y a 12 pentagones et chaque arête est commune à deux pentagones -> 5x12/2 = 30 arêtes.
Donc F=12, S=20, A=30
L'icosaèdre dual du dodécaèdre -> on remplace les sommets par des faces et réciproquement
S = 12
F = 20
A inchangé. On vérifie :
20 faces avec 3 côtés communs
A = 20x3/2 = 30
Dans les deux cas, la somme S+F+A est la même (62).
4 ...
Ça m'suffit pour le moment
.

Tchernobilly the kid- Messages : 947
Date d'inscription : 11/07/2016
Age : 76
Localisation : midi moins le quart
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Oui, c'est bien, Tcherno !
A propos de fullerènes, savez-vous que d'autres abeilles ont construit sur un grosse sphère un début de ruche alvéolé qu'elles ont appelé "Full Reine" pour faire plaisir à leur maman

Et, savez-vous combien d'alvéoles sont pentagonales dans ce méga-polyèdre à 540 sommets ?
A propos de fullerènes, savez-vous que d'autres abeilles ont construit sur un grosse sphère un début de ruche alvéolé qu'elles ont appelé "Full Reine" pour faire plaisir à leur maman

Et, savez-vous combien d'alvéoles sont pentagonales dans ce méga-polyèdre à 540 sommets ?

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
à vue de nez, je dirais 8 ...
.
.

Tchernobilly the kid- Messages : 947
Date d'inscription : 11/07/2016
Age : 76
Localisation : midi moins le quart
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Je ne sais pas, Tcherno, si c'est 8...
Nous, les épis, ne savons pas tout !
Cependant nous avons nos ingénieurs...
Vous avez vu que dans la vidéo, le ballon d'Adidas en 6 pièces est assimilable à un cube (à 6 faces).

Et bien, nos épis ingénieurs ont réussi à faire un ballon en 2 pièces !

J'expliquerais plus tard, dans un autre devoir, ce à quoi cela correspond dans la nature, tout au moins dans le principe, à une échelle beaucoup plus petite, pour nous les épis.
Nous, les épis, ne savons pas tout !
Cependant nous avons nos ingénieurs...
Vous avez vu que dans la vidéo, le ballon d'Adidas en 6 pièces est assimilable à un cube (à 6 faces).

Et bien, nos épis ingénieurs ont réussi à faire un ballon en 2 pièces !

J'expliquerais plus tard, dans un autre devoir, ce à quoi cela correspond dans la nature, tout au moins dans le principe, à une échelle beaucoup plus petite, pour nous les épis.

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Tcherno !
J'ai regardé attentivement le fullerène 540
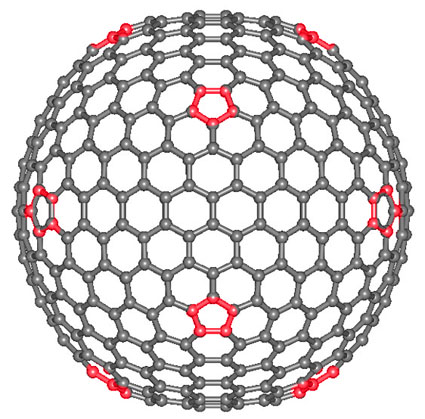
En coloriant les pentagones pour bien les voir, on remarque alors qu'ils sont disposés en losange et on comprend, en regardant leurs orientations respectives que la structure cristalline correspondante est le dodécaèdre à faces losanges dont les diagonales ont un rapport des longueurs égal à √2. Il y a donc 14 pentagones disposés en "1 - 4 - 4 - 4 - 1".
Notons que ce dodécaèdre est le dual du cuboctaèdre que nous étudierons dans le devoir de géométrie N°4.
La réponse à la question 4 est :
Tous les polyèdres convexes respectent l'égalité "S + F = A + 2".
Dans le cas du fullerène 540 représenté ci-dessus, nous avons, je pense :
F = 284
S = 540 (atomes de carbone)
A = 822 (ça en fait des liaisons covalentes !)
La suite au prochain numéro !
J'ai regardé attentivement le fullerène 540

En coloriant les pentagones pour bien les voir, on remarque alors qu'ils sont disposés en losange et on comprend, en regardant leurs orientations respectives que la structure cristalline correspondante est le dodécaèdre à faces losanges dont les diagonales ont un rapport des longueurs égal à √2. Il y a donc 14 pentagones disposés en "1 - 4 - 4 - 4 - 1".
Notons que ce dodécaèdre est le dual du cuboctaèdre que nous étudierons dans le devoir de géométrie N°4.
La réponse à la question 4 est :
Tous les polyèdres convexes respectent l'égalité "S + F = A + 2".
Dans le cas du fullerène 540 représenté ci-dessus, nous avons, je pense :
F = 284
S = 540 (atomes de carbone)
A = 822 (ça en fait des liaisons covalentes !)
La suite au prochain numéro !

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
... Moi aussi.SansOgm a écrit:Tcherno !
J'ai regardé attentivement le fullerène 540
???
En coloriant les pentagones pour bien les voir, on remarque alors qu'ils sont disposés en losange et on comprend, en regardant leurs orientations respectives que la structure cristalline correspondante est le dodécaèdre à faces losanges dont les diagonales ont un rapport des longueurs égal à √2. Il y a donc 14 pentagones disposés en "1 - 4 - 4 - 4 - 1".
Désolé, après avoir mis mes lunettes sur mon nez,qui sans cela en voyait 8, j'en vois finalement 12 !
Disposés par 4 sur 3 grands cercles "orthogonaux" (comme l'équateur et les méridiens 0°/180° et 90°/-90°
Et c'est mon dernier mot, Jean-Pierre !
C'est effectivement ce qu'après petite recherche on trouve sur de bons sites Internet sous le nom de théorème de Descartes-EulerLa réponse à la question 4 est :
Tous les polyèdres convexes respectent l'égalité "S + F = A + 2".
http://villemin.gerard.free.fr/Wwwgvmm/Geometri/Polyedre.htm#Euler
.

Tchernobilly the kid- Messages : 947
Date d'inscription : 11/07/2016
Age : 76
Localisation : midi moins le quart
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
SansOgm,
je confirme, vous vous vourfoyez avec vos 14 pentagones.
Nous les humains les avons bien étudiés, il n'y en a que 12 !
Voici ce que nous savons des fullerènes :
---------------------------
Pour qu'un fullerène soit stable, les anneaux pentagonaux ne doivent pas être adjacents. D'une façon générale, on définit les fullerènes C2n comme étant des structures fermées composées de (2n-20)/2 hexagones et de 12 pentagones. La plus petite molécule sphérique répondant à cette définition est le C60, dont les atomes sont aux sommets d'un icosaèdre tronqué. C'est également le fullerène le plus fréquent. Les fullerènes C60 cristallisent dans le système cubique faces centrées (cfc). Le solide obtenu, à la différence du diamant et du graphite, est un solide moléculaire (cohésion cristalline de type Van der Waals), et chaque molécule C60 peut tourner librement sur elle-même.
En termes mathématiques, la structure d’un fullerène est un polyèdre convexe trivalent avec des faces pentagonales et hexagonales. En théorie des graphes, le terme « fullerène » fait référence à tout graphe planaire régulier-3 avec toutes les faces d’une taille de 5 ou 6 (y compris la face externe). Cela correspond à la caractéristique d'Euler concernant les polyèdres, |V|-|E|+|F| = 2, (où |V|, |E| et |F| indiquent le nombre de sommets, côtés et faces), c'est-à-dire qu’il y a exactement 12 pentagones dans un fullerène et |V|/2-10 hexagones.
---------------------------
Mais, peut-être que vos abeilles et leur "Full Reine" ont réussi à faire 14 pentagones...
Nous en doutons.
je confirme, vous vous vourfoyez avec vos 14 pentagones.
Nous les humains les avons bien étudiés, il n'y en a que 12 !
Voici ce que nous savons des fullerènes :
---------------------------
Pour qu'un fullerène soit stable, les anneaux pentagonaux ne doivent pas être adjacents. D'une façon générale, on définit les fullerènes C2n comme étant des structures fermées composées de (2n-20)/2 hexagones et de 12 pentagones. La plus petite molécule sphérique répondant à cette définition est le C60, dont les atomes sont aux sommets d'un icosaèdre tronqué. C'est également le fullerène le plus fréquent. Les fullerènes C60 cristallisent dans le système cubique faces centrées (cfc). Le solide obtenu, à la différence du diamant et du graphite, est un solide moléculaire (cohésion cristalline de type Van der Waals), et chaque molécule C60 peut tourner librement sur elle-même.
En termes mathématiques, la structure d’un fullerène est un polyèdre convexe trivalent avec des faces pentagonales et hexagonales. En théorie des graphes, le terme « fullerène » fait référence à tout graphe planaire régulier-3 avec toutes les faces d’une taille de 5 ou 6 (y compris la face externe). Cela correspond à la caractéristique d'Euler concernant les polyèdres, |V|-|E|+|F| = 2, (où |V|, |E| et |F| indiquent le nombre de sommets, côtés et faces), c'est-à-dire qu’il y a exactement 12 pentagones dans un fullerène et |V|/2-10 hexagones.
---------------------------
Mais, peut-être que vos abeilles et leur "Full Reine" ont réussi à faire 14 pentagones...
Nous en doutons.

saint-marc- Messages : 852
Date d'inscription : 05/09/2016
Age : 66
Localisation : Poitiers
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Hé ! les enfants, ne vous acharnez pas contre moi !
Je vous ai dit que nous, les épis de maïs, ne savions pas tout. Et, d'ailleurs, je trouve passionnant que nous puissions coopérer. Pour les calculs, comprenez bien que ce n'est pas facile pour nous... nos bouliers à grains ne sont pas parfaits.
Mais, je compte sur vous pour partager nos connaissances :
Je vous ai dit que nous, les épis de maïs, ne savions pas tout. Et, d'ailleurs, je trouve passionnant que nous puissions coopérer. Pour les calculs, comprenez bien que ce n'est pas facile pour nous... nos bouliers à grains ne sont pas parfaits.
Mais, je compte sur vous pour partager nos connaissances :
L'alliance nouvelle "humaïs" va faire des épeautres !


D'ailleurs, je compte sur vous pour fignoler notre proposition de ballon à deux pièces : ça fera un tabac l'été prochain, en bord de mer ! (et oui, ça fume...)

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
SansOgm a écrit:
Mais, je compte sur vous pour partager nos connaissances :
OK, je peux te passer ma recette de pop corn;

je compte sur vous pour fignoler notre proposition de ballon à deux pièces
Voici le deux pièces de base, reste à faire le pavage en mode fullerène.

 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Monsieur Gaston,
ne provoquez pas systématiquement notre ami SansOgm : Il a le sang zaud ! (j'aime !)
J'en veux pour preuve toutes vos remarques sarcastiques :
1- Dodécaèdre à 12 faces : Hein ? fallait-il l'humilier ?
2- Y-a pas que des carbones : Comme dirait nos voisins british,
Des molécules en forme de ballon de football, ou fullerènes, formées d'atomes de bore ont été observées. Jusqu’à présent, on ne connaissait que des fullerènes de carbone.
Le borosphérène est une molécule, en forme de cage à peu près sphérique, qui comporte 40 atomes de bore. (Materialscientist/Wikicommons)
Les fullerènes ont été découverts en 1985. La plus connue de ces molécules sphériques est celle comportant 60 atomes de carbone (C60), qui reproduit la structure de la surface d'un ballon de football. Des variantes avec plus ou moins d’atomes ont depuis été synthétisées, toutes constituées de carbone. Est-il possible de fabriquer des fullerènes avec un autre élément ? La question est d’autant plus intéressante que les fullerènes de carbone ont trouvé de nombreuses applications en chimie et dans les nanotechnologies. Une équipe de chimistes de l’Université Brown, aux États-Unis, et de trois universités chinoises, vient de mettre en évidence l'existence de fullerènes formés de 40 atomes de bore.
Le bore précède le carbone dans le tableau périodique des éléments ; il a donc un électron de moins. Ainsi, les chimistes pensaient qu’une structure comportant 60 atomes de bore similaire au fullerène C60 serait instable. Toutefois, des calculs suggéraient qu'une structure formée de 80 atomes de bore pouvait être plus stable.
Lai-Sheng Wang, de l’Université Brown, et ses collègues, étudient les structures de bore depuis près de dix ans. Ils avaient déjà réussi à fabriquer des molécules en forme de disque composées d'un grand nombre d'atomes de bore, et constaté que certains amas de 40 atomes de bore étaient stables. Mais ils n’avaient pas encore identifié la structure de ces molécules B40.
Pour ce faire, ils ont commencé par mesurer le spectre des énergies de liaison de la molécule. Ce spectre est une sorte d'« empreinte digitale » de la molécule, caractéristique de chaque arrangement. Ils ont ensuite simulé sur ordinateur 10 000 arrangements possibles de ces 40 atomes. De ces modèles, les chimistes ont extrait le spectre d'énergies de liaison associé à chaque structure.
Pour obtenir le spectre expérimental, les chercheurs commencent par préparer un gaz d’atomes de bore, rapidement refroidi pour former de petits amas d’atomes. Les ensembles comportant 40 atomes sont sélectionnés grâce à un spectromètre de masse. Ces molécules sont ensuite irradiées par un laser qui leur arrache un électron. On détermine alors le spectre d’énergie des liaisons à partir de la vitesse des électrons arrachés, une technique nommée spectrométrie de photoélectrons.
En comparant les spectres théoriques avec ceux obtenus expérimentalement, L.-S. Wang et son équipe ont montré que des molécules stables de type fullerène comptant 40 atomes de bore s'étaient formées. Ces « sphères » ne sont cependant pas aussi régulières que le fullerène C60 : elles comportent 48 triangles, deux hexagones (en haut et en bas de la structure), et quatre heptagones occupant les côtés. Les chimistes ont nommé cette structure borosphénène.
Il est encore trop tôt pour envisager les applications de ces fullerènes de bore. La prochaine étape sera de mesurer leurs propriétés. En particulier, L.-S. Wang et son équipe veulent étudier les interactions du fullerène de bore et l’hydrogène, qui pourrait être forte car le bore présente un déficit en électrons comparé au carbone. Ce fullerène de bore pourrait ainsi être un bon candidat pour stocker le dihydrogène dans les piles à combustible.
Finalement, cette collaboration toute enfumée est intéressante !
Pour le ballon 2 pièces, que dites-vous, SansOgm, d'une matière imprimée en 3D comme celle-là ?

ne provoquez pas systématiquement notre ami SansOgm : Il a le sang zaud ! (j'aime !)
J'en veux pour preuve toutes vos remarques sarcastiques :
1- Dodécaèdre à 12 faces : Hein ? fallait-il l'humilier ?
2- Y-a pas que des carbones : Comme dirait nos voisins british,
Mister SansOgm is gonna get bored
3- Et pas que que lui, même ses fullerènes !
Tiens ! ça n'a pas tardé...Des fullerènes de bore
Des molécules en forme de ballon de football, ou fullerènes, formées d'atomes de bore ont été observées. Jusqu’à présent, on ne connaissait que des fullerènes de carbone.

Les fullerènes ont été découverts en 1985. La plus connue de ces molécules sphériques est celle comportant 60 atomes de carbone (C60), qui reproduit la structure de la surface d'un ballon de football. Des variantes avec plus ou moins d’atomes ont depuis été synthétisées, toutes constituées de carbone. Est-il possible de fabriquer des fullerènes avec un autre élément ? La question est d’autant plus intéressante que les fullerènes de carbone ont trouvé de nombreuses applications en chimie et dans les nanotechnologies. Une équipe de chimistes de l’Université Brown, aux États-Unis, et de trois universités chinoises, vient de mettre en évidence l'existence de fullerènes formés de 40 atomes de bore.
Le bore précède le carbone dans le tableau périodique des éléments ; il a donc un électron de moins. Ainsi, les chimistes pensaient qu’une structure comportant 60 atomes de bore similaire au fullerène C60 serait instable. Toutefois, des calculs suggéraient qu'une structure formée de 80 atomes de bore pouvait être plus stable.
Lai-Sheng Wang, de l’Université Brown, et ses collègues, étudient les structures de bore depuis près de dix ans. Ils avaient déjà réussi à fabriquer des molécules en forme de disque composées d'un grand nombre d'atomes de bore, et constaté que certains amas de 40 atomes de bore étaient stables. Mais ils n’avaient pas encore identifié la structure de ces molécules B40.
Pour ce faire, ils ont commencé par mesurer le spectre des énergies de liaison de la molécule. Ce spectre est une sorte d'« empreinte digitale » de la molécule, caractéristique de chaque arrangement. Ils ont ensuite simulé sur ordinateur 10 000 arrangements possibles de ces 40 atomes. De ces modèles, les chimistes ont extrait le spectre d'énergies de liaison associé à chaque structure.
Pour obtenir le spectre expérimental, les chercheurs commencent par préparer un gaz d’atomes de bore, rapidement refroidi pour former de petits amas d’atomes. Les ensembles comportant 40 atomes sont sélectionnés grâce à un spectromètre de masse. Ces molécules sont ensuite irradiées par un laser qui leur arrache un électron. On détermine alors le spectre d’énergie des liaisons à partir de la vitesse des électrons arrachés, une technique nommée spectrométrie de photoélectrons.
En comparant les spectres théoriques avec ceux obtenus expérimentalement, L.-S. Wang et son équipe ont montré que des molécules stables de type fullerène comptant 40 atomes de bore s'étaient formées. Ces « sphères » ne sont cependant pas aussi régulières que le fullerène C60 : elles comportent 48 triangles, deux hexagones (en haut et en bas de la structure), et quatre heptagones occupant les côtés. Les chimistes ont nommé cette structure borosphénène.
Il est encore trop tôt pour envisager les applications de ces fullerènes de bore. La prochaine étape sera de mesurer leurs propriétés. En particulier, L.-S. Wang et son équipe veulent étudier les interactions du fullerène de bore et l’hydrogène, qui pourrait être forte car le bore présente un déficit en électrons comparé au carbone. Ce fullerène de bore pourrait ainsi être un bon candidat pour stocker le dihydrogène dans les piles à combustible.
Finalement, cette collaboration toute enfumée est intéressante !
Pour le ballon 2 pièces, que dites-vous, SansOgm, d'une matière imprimée en 3D comme celle-là ?

Dernière édition par saint-marc le Mer 23 Nov - 19:19, édité 1 fois

saint-marc- Messages : 852
Date d'inscription : 05/09/2016
Age : 66
Localisation : Poitiers
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
Merci les amis !
Tant de collaboration me fait chaud aux grains.
C'est curieux, nous les épis nous sommes également inspiré d'un accessoire féminin pour trouver notre ballon à 2 pièces. Cet accessoire est le suivant

Il est encore trop tôt pour vous expliquer tout cela, nous ferons un devoir complet sur le ballon à 2 pièces.
Tant de collaboration me fait chaud aux grains.
C'est curieux, nous les épis nous sommes également inspiré d'un accessoire féminin pour trouver notre ballon à 2 pièces. Cet accessoire est le suivant

Il est encore trop tôt pour vous expliquer tout cela, nous ferons un devoir complet sur le ballon à 2 pièces.

SansOgm- Behavioral Analysis Unit

- Messages : 104
Date d'inscription : 27/09/2016
 Re: 03-Devoir de géométrie N°3
Re: 03-Devoir de géométrie N°3
SansOgm, avant qu'on aborde les p'tites serviettes de ces dames, puisqu'on parle de bore, je souhaite vous faire profiter d'un tuyau :

Si vous fouanez des arpions, utilisez des paillettes d'acide borique


saint-marc- Messages : 852
Date d'inscription : 05/09/2016
Age : 66
Localisation : Poitiers
 Sujets similaires
Sujets similaires» 05-Devoir de géométrie N°4
» 06-Devoir de géométrie N°5
» 09-Devoir de géométrie N°6
» 12-Devoir de géométrie N°7
» 01-Devoir de géométrie N°1
» 06-Devoir de géométrie N°5
» 09-Devoir de géométrie N°6
» 12-Devoir de géométrie N°7
» 01-Devoir de géométrie N°1
Page 1 sur 1
Permission de ce forum:
Vous ne pouvez pas répondre aux sujets dans ce forum|
|
|

 Voir les nouveaux sujets
Voir les nouveaux sujets Voir les sujets sans réponse
Voir les sujets sans réponse


» forum actif
» collection complète san antonio
» COLLECTION COMPLETE DE SAN ANTONIO
» Collection complète des San-Antonio (Frédéric Dard) en e-books
» san antonio téléchargement e pub ou pdf
» Liens pour la colection San-Antonio
» San Antonio
» Collection e-book San Antonio .
» Monoc Chauvin & Arnoux (et Métrix 202) substitution de pile
» san antonio
» Capacité de decharge batterie outillage elctro portatif type Makita
» collection compete san antonio
» Pourquoi dit-on ? Lâcher une Louise
» batterie iphone se décharge en 12h, top neuve!
» The universal anesthesia machine ! l'avis d'Aelyta m'intéresse.
» "Vaccinez-vous, braves gens ! vaccinez-vous"! En clair : "Alertes aux citoyens, vaccinés ou non, sur l’état actuel des conséquences vaccinales" !
» Traducteur de textes longs
» DIFFERENCES ENTRE CE FORUM ET YAHOO Q/R - NOUVEAUX UTILISATEURS LISEZ CETTE SECTION
» L'imagination ne surpasse t-elle pas la pensée ?
» La machine ENIGMA Version simulateur tutoriel partie1
» SIMULATEUR MACHINE ENIGMA
» Nouvel utilisateur ? Pour terminer votre inscription ouvrez ce topic
» C'est décidé, le BC603 avec sa convertisseuse dynamotor dm 34 va reprendre du service !
» A l'attention de Pierre, étude d'un récepteur tube en HT 25V
» Changez vos DNS si vous ne voulez plus être espionné par Google !
» Générateur de signal à 1Hz
» Les batteries lithium-ion, principe et utilisation
» Etrange incendie de la cathédrale !
» Pourquoi se polit-on le chinois et pas le hollandais ?
» VOUS ETES MEMBRE ? LISEZ MOI !
» (Politique/événement) A propos du Brexit
» moteur 1500 tours alimenté en 1V pour 30 µA
» C'est Pâques, alors... j'arrive !
» Escroc !!
» Montage Batteries Lithium Ion 3,7 * 2
» Financement - Post mis à la benne !
» pour animer Brest et devenir chaleureuse
» "use the force luke" essayez c'est rigolo : Mode d'emploi
» batterie rechargable defectueuse
» Chargeur d'accus Li-Ion CACA !
» Générateur de signal à 1Hz Seconde partie
» Grid Dip UHF...
» Quand une année finit, une autre prend le relais
» Les pétitions : Valeur juridique, utilité, dangers et la pétition par internet vs pétition papier
» Traitement du bois
» Bloctel : Etes-vous déjà inscrit sur le site mis à disposition par le gouvernement ?
» Petite formation à l'argomuche de Paname.
» JETEZ PLUS VOS LECTEURS DE DISQUETTE ON FAIT DE LA MUSIQUE AVEC !
» Et si on enseignait l'évolution par des travaux pratiques au lieu de se contenter de la théorie?